具有高空間分辨率和力靈敏度的納米壓痕技術廣泛用于測量硬質生物材料和組織的機械性能。然而,其分析軟生物材料和器官的可靠性尚未經過測試。在這里,我們評估了納米壓痕測量軟生物標本的被動力學性能的效用。從C57BL / 6 N小鼠中收獲腎臟,肝臟,脾臟和子宮樣品。我們使用Bland-Altman圖,類內相關系數(ICC)和受試者內變異系數(COV)評估了生物標本和水凝膠對照中的測試-復測試重復性。結果使用Hertzian,JKR和Oliver & Pherr模型計算得出。與水凝膠類似,所有生物標本的Bland-Altman圖在剛度測試和復試檢查中表現出良好的可靠性。在所有三種模型中,ICC均大于0.8,COV小于15%。在腎臟,肝臟,脾臟和子宮中,ICC僅在Hertzian模型中始終大于0.8,而在JKR和Oliver & Pherr模型中則不然。同樣,僅在赫茲模型中腎臟、肝臟、脾臟和子宮的COV始終小于15%,而在其他模型中則不然。我們得出結論,納米壓痕技術在檢測腎臟,肝臟,脾臟和子宮的硬度方面是可行的。赫茲模型是提供所研究生物標本離體器官剛度可靠結果的方法。
從5周,10周,20周和30周齡C57BL / 6 N小鼠解剖腎臟,肝臟和脾臟。對于腎臟和脾臟,使用每種性別和年齡的2只小鼠。對于肝臟,使用每種性別和年齡的2至4只小鼠。對于子宮,使用了八只小鼠,所有這些小鼠都在100天左右。這些實驗得到了當地動物護理委員會(LAGeSo,德國柏林)和馬克斯·德爾布呂克分子醫學中心(MDC)動物福利官員的批準(編號X 9011/19)。
具有不同剛度的水凝膠(1 kPa,2 kPa,4 kPa,8 kPa,12 kPa和25 kPa)從Softwell,Matrigen,Matrigen Life Technologies,Brea,CA購買,用于質量控制(1 kPa,2 kPa,4 kPa,8 kPa,12 kPa和25 kPa;N = 1 到 3)。
左腎和右腎分別從側中線分為兩個(圖)。3A),四個部分全部縮進。肝臟樣本取自左葉(圖)。四A). 整個收獲脾臟用于實驗(圖)。4選擇并打開左子宮角(圖)。5答,B)。所有器官都經過清潔,去除器官表面可見的血液,脂肪,膜或血管,但避免損壞它們的實質。為了獲得平坦的表面,我們將所有樣品粘貼到直徑為6厘米的培養皿底部,并用蟲膠(Sigma)使外表面平整。將組織樣品浸入PBS(NaCl 4.0 M,KCl 137.0 M,Na2高原油40.01 米,千米2采購訂單40.0018米;酸堿度 7.4)。
為了確定彈性特性,我們使用了位移控制的納米壓痕儀(Piuma;光學11,荷蘭阿姆斯特丹)。該設備采用套圈頂部懸臂探頭32,33施加負載并使用基于光纖的讀數同時測量壓痕深度(圖)。1A). 我們使用半徑為 50 μm 且懸臂剛度為 0.5 N/m 的球形探頭。在每一系列實驗之前,通過壓入剛性表面并將懸臂彎曲等同于探頭位移來進行懸臂彎曲校準。之后,將探針聚焦在組織表面的適當區域(圖。1B、3A、4A、5A、6B)。在25×5 μm網格掃描中,將每個凝膠壓痕5次(800×800個基質),測量間隔距離為200 μm。腎臟、肝臟和脾臟樣品在9××3μm網格掃描中用3個壓痕(200個基質)壓進(圖。200B、3B、4B)。在子宮中,分別在子宮的近端、中部和遠端測試了 5 × 4 μm 網格中具有 100 個單壓痕的三個壓痕矩陣(圖)。100B,C)。應用的壓痕方案由在6 nm壓痕深度下4 s的加載階段(保持8000秒)和卸載階段4 s組成。所有掃描都進行了兩次,以分析可靠性。左右腎四個部分所有結果的平均值表示為腎臟彈性。凝膠、肝臟和脾臟的硬度表示為每次掃描中所有結果的平均值。三次掃描結果的平均值作為子宮硬度。所有單個壓痕值均由 Piuma Dataviewer 版本 2.2 (Piuma;光學11,荷蘭阿姆斯特丹)。
Piuma納米壓痕技術已廣泛應用于硬動物器官的生物材料剛度研究,例如骨骼25、耳內、鼻翼和鼻外隔細胞和細胞外基質 (ECM) 水平24,26,在膝關節22,在關節軟骨中23.其他例子是人類供體角膜27、纖維化腸組織30、胰腺無細胞支架31、軟板28尤其是鈣化的動脈瘤腹主動脈29.該技術在測量軟生物材料,特別是離體器官的剛度方面的可行性和可靠性尚不清楚。與硬質生物材料相比,軟質生物材料的某些性能,如粘彈性和附著力,更容易出現納米壓痕的偏差。我們的研究是第一個使用這項技術在體外測試軟生物器官的剛度,特別是來自小鼠的剛度,這些器官廣泛用于模擬人類和動物疾病。我們應用了Piuma納米壓痕技術,該技術易于使用,并利用特定的探針來測量楊氏模量,以匹配組織的特定樣品特性42,43,44 .不同的組織具有不同的機械性能,因此,應在具有某些特殊特征的組織中應用不同的方案45.由于在實驗前無法判斷被測樣品的特征,因此我們分析了加載和卸載零件的彈性行為檢測。除了系統的運行和測量策略的開發外,組織的制備和固定也非常重要。不規則的組織無法測試,因為該設備只能識別平坦穩定的表面,并且剛度的計算會受到樣品狀況的影響。例如,如果被測表面是斜率(補充1,圖1A),則接觸區域不會被探頭縮進,這意味著失去深度和力可能導致剛度測量錯誤。球狀器官(補充1圖1B)也是不可測試的,因為它在測量過程中不能穩定。此外,由于組織邊緣的障礙物,該技術不可能測試下沉的表面(補充1圖1C)。塊狀表面(補充1圖1D)不僅會影響測量結果的準確性,還會導致探頭懸臂因卡住而損壞。一起,需要以適當的形狀和大小制備可測試的被測組織。我們確實克服了納米壓痕技術的可行性和可靠性的這些可能限制,該技術通過使用以適當方式解剖的孤立腎臟,肝臟,脾臟和子宮來測量軟器官硬度。我們通過對該技術與Matrigen水凝膠的比較研究證實了結果的可行性和可靠性。在給定剛度,穩定形狀,適當厚度和平坦表面的Matrigen水凝膠作為質量控制,盡管它們給定的剛度不被認為是黃金標準。然而,我們的Bland-Altman圖、ICC和COV證明了所用凝膠的良好可靠性。因此,我們得出結論,納米壓痕技術在我們的實驗室環境和這種材料上運行良好且可靠。
接下來,我們測試了該技術在體外測量四個器官的硬度,即腎臟,肝臟,脾臟和子宮。盡管Bland-Altman圖沒有給我們提供許多不合格的結果,但不同模型中四種器官硬度的結果的可靠性只能通過比較ICC和COV來驗證。在四個器官中,所有赫茲模型的結果都遵循ICC的量化標準,COVs顯示出可靠的結果。JKR或Oliver & Pharr模型的結果并不總是符合高質量標準。觀察到差異的原因可能取決于樣品在卸載狀態下的粘性差異。
例如,在JKR模型中,即使在相同的樣品上,一些斑點是粘性的,而一些單個壓痕顯示沒有粘附,如圖所示。1E,這將增加測試和重新測試之間的差異。因此,我們的結果表明,在強制壓痕下,最好使用赫茲模型計算所研究的四個器官的硬度。值得注意的是,該模型已被其他研究人員使用,他們在研究中利用了納米壓痕技術。27,28,29 ,而其他研究沒有報告使用的模型30,31.此外,將子宮與其他三個器官的結果進行比較,我們發現即使在赫茲模式下,根據Eff計算硬度的情況下子宮的COV值為11.6893%,在根據E計算剛度的情況下,子宮的COV值為14.1841%,非常接近閾值,遠高于赫茲模型中其他三個器官的COV值。這表明重復測量子宮之間的差異大于肝臟,腎臟和脾臟的變異性。一個可能的原因是子宮比其他三個器官更小更薄,在實驗過程中,我們發現更小更薄的器官子宮的邊緣更容易卷起,導致類似情況如補充1圖1B所示,預計會影響測量結果。因此,該方法在體外較大較厚的軟器官中的可靠性較好。
此外,納米壓痕的成功應用在很大程度上取決于材料特征,例如被測組織的形狀;測量具有復雜粗糙表面的生物材料往往很困難。當一個組織被手工轉化為可以測試的材料時,不知道它的彈性是否保持與原始器官的彈性相同的性質,以及器官的部分彈性是否可以代表其整體彈性。因此,對于某些器官研究,體內測試可能是提供器官機械性能詳細見解的更好甚至的選擇。然而,體內測試在測量過程中可能會受到其他因素的干擾和影響,因此納米壓痕器可以直接與目標材料接觸進行測量可能是一個優勢。目前,該技術的應用存在較多的局限性和不足。例如,其有效性和真實性仍需進一步驗證,生物材料納米壓痕的標準化程序尚未建立。因此,我們不能肯定它是否會成為軟器官和組織機械生物學和生物力學研究中的工具。然而,隨著這項技術的研發越來越深入,我們預計它將有很大的機會應用于軟器官生理學和病理學等多個領域的研究。
Piuma納米壓痕技術是一種簡單可行的離體器官硬度測試方法,如腎臟,肝臟,脾臟和子宮。在表面無序的小而薄的組織中,我們預計結果的變化會增加。赫茲模型是體外測量軟器官和生物材料的被動力學性能的方法。JKR和Oliver & Pharr模型沒有提供可靠的結果。
原文鏈接:評估納米壓痕在軟生物材料硬度測量中的應用:腎臟、肝臟、脾臟和子宮 |科學報告


Piuma是功能強大的臺式儀器,可探索水凝膠、生理組織和生物工程材料的微觀機械特性。表征尺度從宏觀直至細胞。專為分析測試軟材料而設計,測量復雜和不規則材料在生理條件下的力學性能。杭州軒轅科技有限公司
● 內置攝像鏡頭,方便實時觀察樣品臺
● 實時分析計算測量結果,原始數據并將以文本文件存儲,方便任何時候導入Dataviewer軟件進行復雜處理
● 探針經過預先校準,即插即用。對于時間敏感的樣品確保了快速測量
● 光纖干涉MEMS技術能夠以無損的方式測量即使是最軟的材料,并保證分辨率。同時探針可以重復使用Piuma軒轅納米壓痕儀Piuma軒轅納米壓痕儀
| 模量測試范圍 | 5 Pa - 1 GPa |
| 探頭懸臂剛度 | 0.025 - 200 N/m |
| 探頭尺寸(半徑) | 3 - 250 μm |
| 最大壓痕深度 | 100 μm |
| 傳感器最大容量 | 200 |
| 測試環境 | air, liquid (buffer/medium) |
| 粗調行程 | X*Y:12×12 mm Z:12 mm |
加載模式 | Displacement / Load* / Indentation* |
| 測試類型 | 準靜態(單點,矩陣) 蠕變,應力松弛 DMA動態掃描 (E', E'', tanδ) |
| 動態掃描頻率* | 0.1 - 10 Hz |
| 內置擬合模型 | Young's Modulus (Hertz / Oliver-Pharr / JKR) |
| *為可選升級配置 | |
新型光纖干涉式懸臂梁探頭,利用干涉儀來監測懸臂梁形變。
創新型光纖探頭,彌補了傳統納米壓痕儀無法測試軟物質的問題,也解決了AFM在力學測試中的波動大,操作困難、制樣嚴苛等常見缺陷。
● 背景噪音低:激光干涉儀抗干擾強于AFM反射光路
● 制樣更簡單:對樣品的粗糙度寬容度高于AFM
● 剛度選擇更準確:平行懸臂梁結構有利于準確判別壓痕深度與壓電陶瓷位移比例關系,便于選擇合適剛度探頭來保證彈性形變關系的穩定性,進而獲得重復率更高、準確性更好的數據
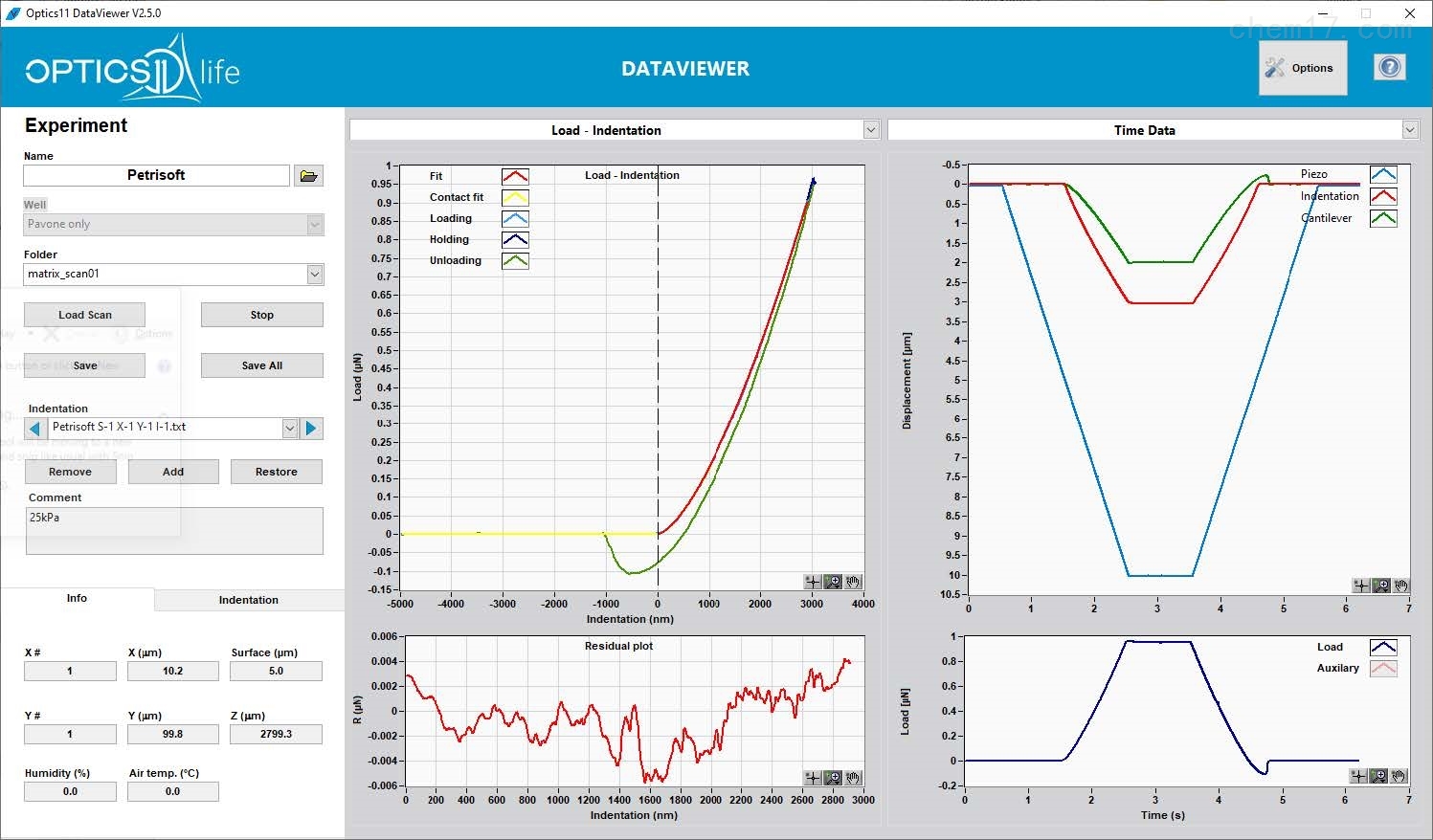
● 借助功能強大而易于操作的軟件,用戶可以自由控制壓痕程序(載荷、位移等)。自動處理曲線的流程,可以獲得數據和結果的快速分析
● 原始參數完整txt導出,便于后續復雜處理的需要
● 利用Hertz接觸模型從加載部分計算彈性模量,與常用的Oliver&Pharr方法相比,更為適合生物組織和軟物質材料特性
| 年 份 | 期 刊 | 題 目 |
|---|---|---|
| 2022 | Advanced Functional Materials | Engineering Vascular Self-Assembly by Controlled 3D-Printed Cell Placement |
| 2022 | Biomaterials | Hydrogels derived from decellularized liver tissue support the growth and differentiation of cholangiocyte organoids |
| 2021 | Biofabrication | 3D bioprinting of tissue units with mesenchymal stem cells, retaining their proliferative and differentiating potential, in polyphosphate-containing bio-ink |
| 2021 | nature communications | Janus 3D printed dynamic scaffolds for nanovibration-driven bone regeneration |
| 2020 | Environmental Science & Technology | Effect of Nonphosphorus Corrosion Inhibitors on Biofilm Pore Structure and Mechanical Properties |
| 2020 | Acta Biomaterialia | A multilayer micromechanical elastic modulus measuring method in ex vivo human aneurysmal abdominal aortas |